Nome:
Entregar até 29/09/2016
Atividade referente ao 3º Bimestre – 2ºA –EE Geraldo
1-Coloque i para compostos iônicos, C para os covalentes e m para os metálicos:
a)NaBr ( ) d) SO2 ( ) g) SO3 ( )
b) BF3 ( ) e) CO2 ( ) H) H2SO4 ( )
c) H2O ( ) f) C6H12O6 ( )
2- O que é eletronegatividade? O que são íons?
3- O latão é uma liga de cobre e zinco, essa ligação é iônica, covalente ou metálica?
4-Explique o que são moléculas polares e apolares e dê exemplo.
5- Dê a nomenclatura:
a)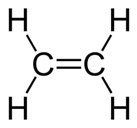 b)
b)
5- Dê a nomenclatura:
a)
 b)
b)
1: a)i b)c c)c d á h são C(covalente)
ResponderExcluir2) Eletronegatividade é a capacidade que um átomo tem de atrair elétrons para si.Íons quando um átomo ganha ou perde elétrons.
3)É uma ligação metálica
4)Polaridade das Moléculas
Durante as ligações químicas, podem sobrar elétrons do átomo central.
Então:
- molécula polar – quando não sobram elétrons do átomo central.
- molécula apolar – quando sobram elétrons do átomo central.
água polar e gás carbônico apolar
5)a)eteno b)hexano